Anvisa aprova Mounjaro Multidose no Brasil; entenda a diferença
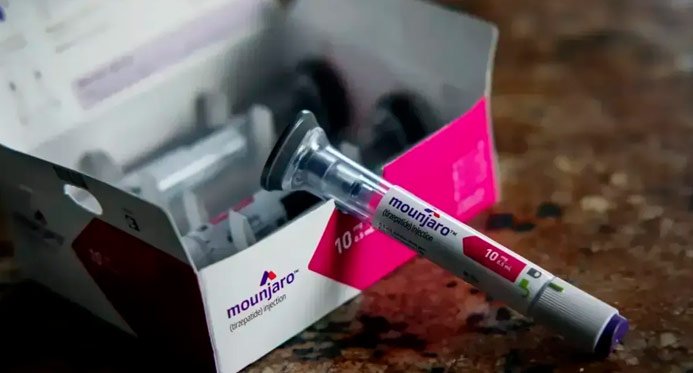
Um novo formato do Mounjauro, medicamento indicado para o tratamento do diabetes tipo 2, recebeu aprovação da Filial Pátrio de Vigilância Sanitária (Anvisa). O cadastro foi confirmado por meio de publicação no Quotidiano Solene da União desta quarta-feira (18).
Diferentemente do protótipo tradicional, que é descartável posteriormente um único uso, a novidade apresentação, chamada Mounjaro Multidose, foi pensada para que o paciente possa utilizar a mesma caneta aplicadora para mais de uma ração.
Entenda o que foi sancionado
Conforme consta na Solução-RE nº 1.041, da Gerência Universal de Medicamentos da Anvisa, o registro foi outorgado à farmacêutica Eli Lily do Brasil, para medicamento à base de tirzepatida.
O aval da filial abrange seis dosagens diferentes do resultado, distribuídas em solução injetável para governo sob a pele (subcutânea). De combinação com a lei, o registro é válido por 24 meses.
- 4,17mg/mL
- 8,33mg/mL
- 12,5mg/mL
- 16,7mg/mL
- 20,8mg/mL
- 25 mg/mL
Principais mudanças
Na prática, a principal mudança está no formato, por isso a novidade versão permite que uma única caneta seja utilizada em diversas aplicações.
Em resumo, a tirzepatida atua nos hormônios relacionados à glicose e ao controle do gosto. Segundo o Ministério da Saúde, é indicado em conjunto com dieta hipocalórica e aumento da atividade física para controle crônico do peso, incluindo perda e manutenção do peso em condições específicas.
Share this content:











Publicar comentário